![]()
Το Η είναι το πιο απλό άτομο που υπάρχει, με ένα πρωτόνιο και ένα ηλεκτρόνιο. Το ηλεκτρόνιο αυτό κινείται κάτω από την επίδραση του δυναμικού του πυρήνα. Το δυναμικό αυτό ισούται με
![]()
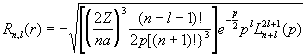
Οπως βλέπουμε οι ακτινικές κυματοσυναρτήσεις εξαρτώνται μόνο από την τιμή του r και από τους κβαντικούς αριθμούς n και l. Η φυσική σημασία της παρατήρησης αυτής είναι ότι η συνάρτηση αυτή καθορίζει τη σχέση ανάμεσα στην απόσταση από τον πυρήνα και την πυκνότητα πιθανότητας εύρεσης του ηλεκτρονίου στην απόσταση αυτή.
Οι γωνιακές κυματοσυναρτήσεις (ονομάζονται
και σφαιρικές αρμονικές) εξαρτώνται από τις γωνίες φ και
θ
καθώς και από τους l και m κβαντικούς αριθμούς. Η φυσική
σημασία των γωνιακών συναρτήσεων είναι ότι ορίζουν το σχήμα του τροχιακού
στο χώρο.
Τα τρισδιάστατο γράφημα τους σε πολικές συντεταγμένες φαίνονται παρακάτω
s 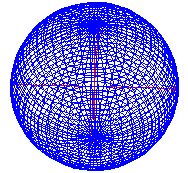
px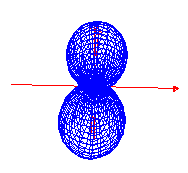 py
py pz
pz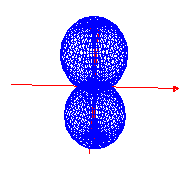
dz2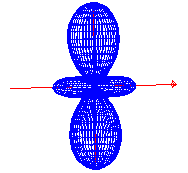 dzx
dzx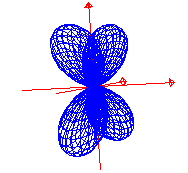 dyz
dyz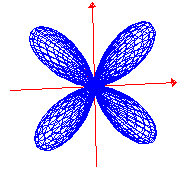 dx2-y2
dx2-y2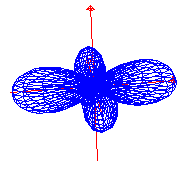
dxy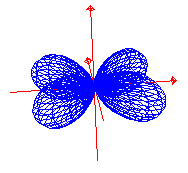
Το γινόμενο των ακτινικών κυματοσυναρτήσεων με τις σφαιρικές αρμονικές
δίνουν τα ατομικά τροχιακά για το υδρογόνο.
Υπολογισμοί
Υπολογισμοί για τις ακτινικές κυματοσυναρτήσεις μπορούν
να γίνουν με το πρόγραμμα radi
.
Η μορφή των ατομικών τροχιακών του Η μπορεί να δωθεί από το πρόγραμμα
contour